検査順位を考える際の原則として、以下を優先する項目として挙げている書籍1)があります。
・ 得られる臨床情報が重要な検査
・ 有効半減期の短い放射性医薬品
・ γ線エネルギーの低い放射性核種
・ 投与量の少ない放射性医薬品
・ 一方の放射性医薬品の体内分布が、他方の検査に影響をおよぼす可能性が低い検査
投与間隔の目安を表に示します1,2)。
d:日(1d=24時間) h:時間 m:分 s:秒 空欄:同日可能
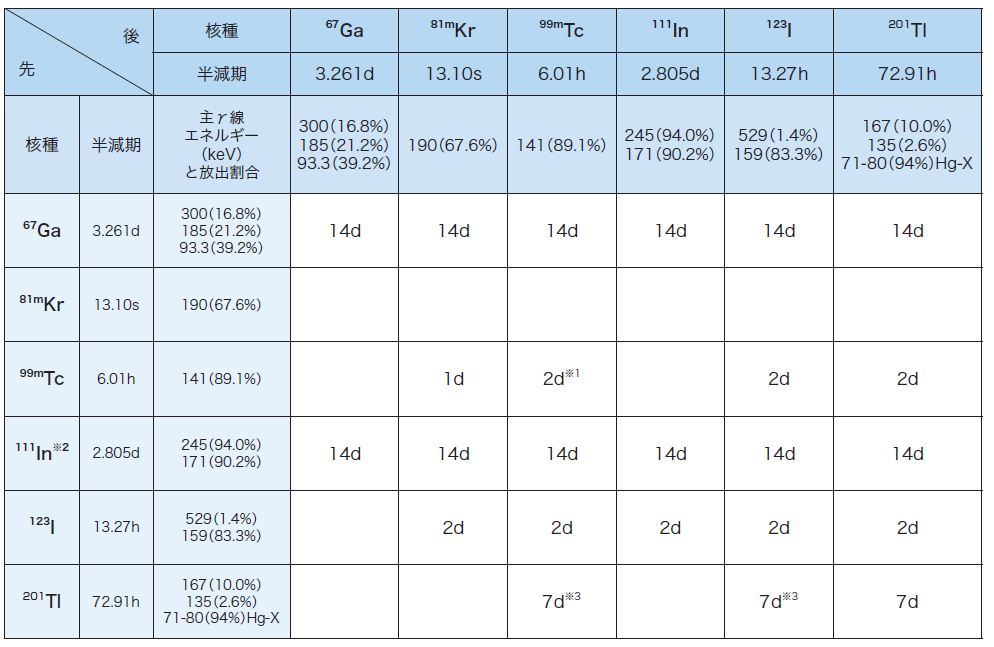
※1 : 99mTc標識薬剤投与後に99mTcO4-を投与する場合、99mTc標識薬剤に含まれるスズイオン(Sn2+)により体内で99mTc標識赤血球が形成され、血液プール像となる可能性があるため、2週間以上間隔をあける3)とされています。
99mTc-DMSAについては、閉塞性尿路障害がなければ99mTc-MAG または99mTc-DTPA検査に続いて検査することができる4)とされています。
※2 : 111In-DTPA投与後の場合は7日空ければ次の検査が可能2)とされています。
※3 : 201Tl検査後の123I製剤、99mTc製剤による検査は定性評価であれば同日に検査可能1)とされています。


 0120-076-941
0120-076-941